密歇根州立大学、约翰霍普金斯大学和斯坦福大学的研究人员合作开发了一种首创的基于纳米粒子的体内成像技术,有朝一日可能用于帮助诊断甚至治疗癌症。
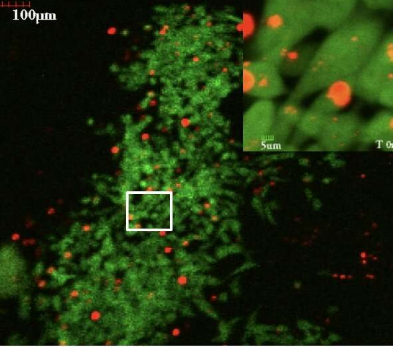
该技术捕捉活体的机械特性,探索物理学与体内(活生物体)生物学之间的基本关系。结果发表在《今日材料》杂志上。
密歇根州立大学生物医学工程副教授 Bryan Smith 与同事合作开发了微小颗粒,一旦进入活细胞内,它们就可以揭示有关细胞结构的重要信息——包括肿瘤细胞在形成肿瘤时如何物理变化。
“我们第一次设计了测量和量化活体动物体内单个活细胞的纳米力学特性的能力,”史密斯说。
在今年早些时候的一项研究中,史密斯和他的团队设计了有助于“吞噬”动脉粥样硬化的纳米颗粒,动脉粥样硬化是动脉中可导致心脏病发作的斑块。这些颗粒选择性地进入称为巨噬细胞的免疫系统细胞,提供一种药物,指导细胞吞噬有害斑块。
现在,史密斯和他的同事们创造了一种使用不同纳米粒子的技术,这些纳米粒子可以嵌入活体动物的各种细胞类型,包括癌性乳腺细胞。分析粒子如何在细胞内移动可以揭示很多有关其内部物理特性的信息。
“以前没有方法可以以高空间分辨率检查活体(例如哺乳动物)的机械特性,”史密斯说。“这种技术有望为疾病诊断和治疗开辟全新的探究途径。”
众所周知,生物组织的机械特性在许多疾病状态中发挥着重要作用,包括心脏病、炎症和癌症,以及正常的生理机能,如细胞迁移和生物体发育。在目前的研究中,Smith 和他的团队首先使用纳米粒子比较培养细胞(标准 2-D 和 3-D)和活体动物细胞之间的机械特性。
跟踪纳米颗粒的运动表明,观察细胞的环境极大地影响了它们的机械性能——这可能意味着某些细胞模型可能不是活体动物的有效代表。
“这告诉对癌症力学感兴趣的癌症科学家,2-D 条件可能很难复制,并且某些 3-D 条件更接近于模拟活小鼠体内的条件,”史密斯说。
实验的下一部分着眼于癌细胞开始形成肿瘤时的内部结构实际发生了什么。以前的方法无法回答这个问题,因为它们的侵入性太大,无法在活体受试者中进行测试。
再次,观察细胞内纳米颗粒的运动,该团队测量了细胞的“柔顺”或柔软程度。重要的是,他们发现正常细胞的柔韧性随着时间的推移保持稳定,但随着癌细胞在一周内形成肿瘤,它们变得僵硬。
“我们发现,当肿瘤开始在活小鼠体内形成时,单个肿瘤细胞会机械地变硬。这是一个基本发现,最终可能对癌症扩散(转移)和肿瘤致死率产生影响,”史密斯说。“通过整合来自我们和我们合作者实验室的最先进的成像和粒子跟踪技术,这一发现成为可能。”
该研究在医学上有许多有前景的应用。其中之一就是简单地评估哪些细胞培养方法足以像活生物体一样提供有意义的信息。另一个是测量生物体中常见生物功能的细胞机械特性,包括器官发育。
史密斯说,也许最令人兴奋的应用可能是疾病诊断和治疗。纳米粒子可用于监测细胞的健康状况以及它们在疾病过程中所经历的变化类型——甚至可能改变这一过程。
史密斯和他的同事计划研究癌症转移的形成和传播,癌症转移导致约 90% 的癌症死亡。
“我希望有一天我们能够治疗转移的物理学,”他说。“但是,我们必须首先了解机制以及改变它们如何影响细胞行为。我们现在正在研究这一点。”